脱发药里的“核武器”,终于来了(美中報道)
一颗缓释口服片,打破近30年的沉寂。Veradermics凭Study302震惊华尔街,背后是8000万患者和一场久违的制剂革命。
4月27日,美国东部时间8点整,Veradermics公司CEO Reid Waldman出现在电话会议中,面对机构投资者和分析师,用一句话开场:我们的Study302临床数据极其的好!
当天,Veradermics的股价(NYSE:MANE)暴涨47.6%,收盘市值突破37亿美元。对于一家零收入的临床阶段生物技术公司,这是一个极其罕见的单日跳升。
但这不仅仅是一个华尔街的故事。在这场数字狂欢的背后,是一个已经等待了近30年的医学难题:什么时候,脱发患者才能吃到一颗真正有效的口服新药?
一份让皮肤科医生震撼的数据
Study302是一项随机、双盲、安慰剂对照的II/III期临床试验,共入组519名轻中度男性雄激素性脱发(AGA)患者,随机分配至VDPHL018.5mg每日一次(QD)、每日两次(BID)或安慰剂组,共治疗6个月。结果出来的那一刻,数字本身就是最好的叙事:
对于两个主要终点
毛发客观增量(TAHC):服用VDPHL01的患者,6个月后BID组增加33.0根/cm²,QD组增加30.3根/cm²,安慰剂组仅7.3根/cm²;相较安慰剂的净增量分别为+25.8根和+23.1根;
患者主观改善(PRO达到“改善”或“明显改善”):BID组62.9%,QD组48.4%,安慰剂组仅13.4%——相当于安慰剂的3.5至4.7倍;
而且,VDPHL01最早在第2个月就观察到了与安慰剂的统计显著分离。
Veradermics在推介PPT中还披露了一项跨试验参照比较(非头对头,需审慎解读):VDPHL01的毛发客观增量(TAHC)为30.3一33根/cm²,而5%米诺地尔泡沫剂是20.9根/cm²,速释口服米诺地尔是10-14.6根/cm²,口服非那雄胺是21.1根/cm²。即便考虑跨试验误差,这一数量级的差距难以被简单归因于偶然。
更让临床医生眼前一亮的,是安全性数据。米诺地尔口服的最大历史顾虑,从来都不是头皮副作用,而是心脏——这种药最初是用来降血压的,口服剂量升高会导致心动过速、水钠潴留,严重时甚至引发心包积液。
Study302给出了令人宽慰的答案:整个试验期间,零例治疗相关严重不良事件,零例心脏来源的特别关注不良事件。不仅如此,因不良事件脱落的患者比例,BID组只有3.4%,实际上低于安慰剂组(3.5%)——这在临床试验设计里,是一个极为罕见的现象。
为什么“缓释”不只是个剂型技巧
要理解VDPHL01为何能同时做到“更有效”和“更安全”,需要先了解一个大多数人不知道的生物学事实:米诺地尔本身,是一个没有活性的前体药物。
它进入人体后,必须在毛囊外根鞘细胞里,被一种叫做SULT1A1的磺基转移酶“激活”——转化为米诺地尔硫酸盐,才能真正打开钾通道、促进毛囊血供、刺激毛乳头细胞增殖。这个酶促过程有两个关键特性:它是容量受限的(酶的处理速度有上限),也是时间依赖的(需要持续的底物供给而非短暂冲击)。
想象一个漏斗:你猛倒一大桶水,大部分溢出去浪费掉;你缓缓注入,漏斗才能充分过滤。米诺地尔的毛囊激活,就是这个漏斗。
这正是普通速释口服米诺地尔的困境所在:吸收快,血药浓度飙升至峰值,心脏开始不舒服;但峰值一过,浓度迅速跌落,毛囊里的酶来不及充分转化,活性代谢物生成有限。
VDPHL01的凝胶基质缓释技术,正是针对性地解决了这一困境。根据公司I期药代动力学数据,VDPHL018.5mg每12小时维持血药浓度在毛囊激活阈值(1.62ng/mL)以上的时间,是2.5mg速释片的2倍;总吸收量(AUC)约翻倍;而峰值浓度(Cmax)被压低到FDA认定的心脏活动阈值(20ng/mL)以下。
简而言之:它把米诺地尔的给药方式,从“猛灌一口”变成了“细水长流”,让毛囊里的限速酶有足够时间把药物转化为真正有用的形式。这是一种制剂层面的精准优化,而非粗暴加量——这也是它能在提升疗效的同时,保持心脏安全性的根本原因。
一位美国社区皮肤科医生在接受Veradermics市场调研的访谈中这样描述:"这是一个更好版本的口服米诺地尔,作为单药治疗更有效,同时维持甚至降低了关键副作用……我会把它形容为一个游戏规则改变者。"
美国现在有多少脱发患者?8000万。其中5000万是男性,3000万是女性。这个数字比湿疹、银屑病和白癜风患者加在一起还要多。
但你知道FDA批准用于AGA的处方药有多少款吗?两款。一款是1987年获批的外用米诺地尔,一款是1997年获批的口服非那雄胺。也就是说,在这29年里,这8000万人的选择,基本上没有变过。
更讽刺的是,这两款药都有显而易见的软肋:外用米诺地尔需要每天在头皮涂抹液体,有研究显示超过86%的女性患者在1年内就停药了——不是因为无效,是因为太烦。非那雄胺则因为性功能副作用的长期顾虑,让大量男性对其望而却步,且该药严格禁用于育龄女性。
结果如何?Veradermics的市场调研数据相当触目惊心:在所有AGA患者中,只有约9%对现有治疗选项表示满意;约46%正在积极寻找新的方案;而在8000万患者里,高达5900万根本没有接受任何治疗。
这是一片等待已久的蓝海。
治疗格局:能打的不多
在AGA这条赛道上,真正的竞争者其实并不多。非那雄胺因为性功能副作用的阴影,在年轻男性市场已经逐渐失去吸引力;外用米诺地尔的依从性问题注定是结构性缺陷;而JAK抑制剂根本就在另一条赛道上——斑秃和AGA,机制截然不同,不能混为一谈。
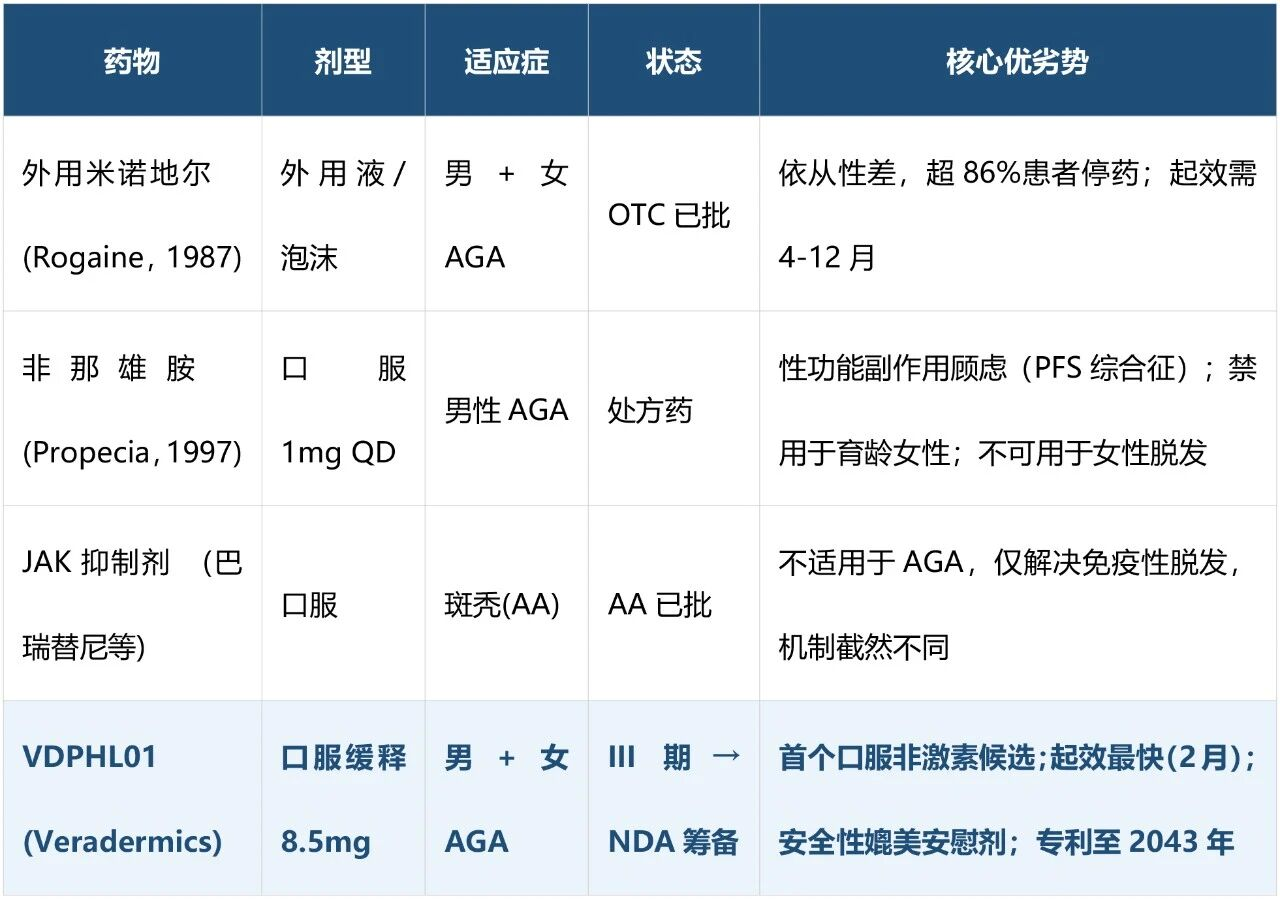
如果VDPHL01最终获批,它面临的不仅是“如何从竞争对手手中抢份额”,而是“如何把那5900万从不治疗的患者带入处方药市场”。后者是一种截然不同的商业逻辑——更接近于市场创造,而非市场竞争。
Veradermics的市场调研数据印证了这一判断:73%的受访皮肤科医生表示有处方VDPHL01的高度意愿,52%的医生预计他们的患者会接受VDPHL01治疗。Jefferies预计VDPHL01上市后可获取约48%的新处方份额,主要从速释口服米诺地尔(off-label)和非那雄胺中切走,同时从根本不治疗的患者群体中开拓增量。
下一站:从数据到药瓶,还有多远
Study302的成功,是一个起点,而不是终点。FDA批准新药,通常需要至少两项设计良好的随机对照试验——Veradermics现在有了第一项。

在整张关键节点图中,接下来最重要的一个节点是Study304——这项入组536名男性的52周确证性III期试验,将在2026年下半年披露顶线数据。它是通往NDA的最后一道关口。一旦Study304复制302的数据质量,NDA提交的大门正式打开,投资者所期待的真正估值重塑才会真正到来。
还有一个被市场低估的价值层:女性适应症。Study306正在为女性AGA患者积极入组——目前在美国这个群体有3000万人,却完全没有任何FDA批准的口服处方选项。若VDPHL01在女性中同样奏效,可将美国市场从5000万扩展至8000万。
中国市场:2.5亿患者,原研新药在哪里?
在中国,脱发是一个比很多人意识到的更严重的问题。国家卫健委数据显示,中国约有2.5亿人受脱发困扰,远超美国的8000万——这是全球最大的单一AGA患者群体。
但中国患者能用的创新处方药,同样屈指可数。国内市场目前仍以米诺地尔仿制药(外用)和非那雄胺仿制药(口服)为主,价格战激烈、产品同质化严重。真正意义上的原创新药研发,在脱发赛道几乎还是一片荒原——直到最近两三年,才开始有值得关注的变化。
苏州开拓药业的KX-826是当前中国最接近商业化的原研脱发新药,也是机制差异化最清晰的选手之一。
KX-826是一种外用雄激素受体(AR)拮抗剂,直接在头皮局部阻断二氢睾酮(DHT)与受体的结合,从源头干预毛囊萎缩过程——而不像非那雄胺那样在系统层面压制整个5-AR通路。这意味着它理论上没有系统性激素副作用,也不存在禁用育龄女性的问题。
3月18日,公司公告关键临床III期达到主要终点。有效性方面:1.0%BID(即每日两次)组和0.5%BID组均较安慰剂组显示出统计学显著的疗效优势及临床意义。1.0%BID组的目标区域TAHC较基线增加15.33根/cm²,0.5%BID组增加14.46根/cm²,安慰剂组增加4.68根/cm²。
尾声:一颗药的时代意义
VDPHL01带来了一种新的创新思路:你不一定需要找到全新的靶点,全新的机制,才能实现临床突破。有时候,把一个已知分子“喂给”患者的方式优化到极致,就足以重写整个赛道的故事。
Study302是一个数据上的里程碑,但更大的考验还在后面。Study304的52周数据、NDA的FDA审批、女性适应症的拓展……每一步都可能带来新的变数,任何一个坏消息都可能引发股价剧烈回调,而这,也正是Biotech投资的永恒张力。
但有一件事,已经可以确定了:脱发这件事,终于可以期待新的治疗选择了。(撰文丨柴妍,医学界)



